Авторы
Панов А. С.
врач психиатр-нарколог, детский реабилитационный центр (филиал)1
Винникова М. А.
д.м.н., профессор кафедры психиатрии и наркологии Института клинической медицины имени Н. В. Склифосовского2
1Государственное бюджетное учреждение здравоохранения города Москвы «Московский научно-практический центр наркологии Департамента здравоохранения города Москвы», 109390, г. Москва, ул. Люблинская, д. 37/1
2Федеральное государственное автономное образовательное учреждение высшего образования Первый Московский государственный медицинский университет
имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский Университет), 119992, г. Москва, ул. Трубецкая, д.8, стр.2
Автор для корреспонденции
Панов Алексей Сергеевич; е-mail: groar@mail.ru
Финансирование
Исследование не имело спонсорской поддержки.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Поступила
16.03.2026
Аннотация
В статье отражены результаты обсервационного одномоментного исследования в области подростковой наркологии. Представлена актуальная информация об употреблении психоактивных веществ (ПАВ) подростками и его связи с полиморфизмом гена DRD2 (rs1800497), кодирующего дофаминовый рецептор 2 типа. Целью работы являлось изучение ассоциации данного генетического маркера с формированием наркологической патологии у лиц подросткового возраста. В исследование включено 188 подростков в возрасте от 15 до 18 лет. Проведен анализ распределения частот генотипов и аллелей, оценена связь носительства аллеля A1 с качественными и количественными показателями потребления различных классов ПАВ, а также с потребностью в стационарном лечении. Установлено, что носители аллеля A1 (генотипы A1/A1 и A1/A2) достоверно чаще пробуют и в последующем злоупотребляют синтетическими каннабиноидами, синтетическими катинонами, галлюциногенами и летучими органическими веществами по сравнению с гомозиготами A2/A2. Выявлен дозозависимый эффект аллеля A1 в отношении употребления синтетических катинонов. Наличие хотя бы одного аллеля A1 ассоциировано с более высокими шансами госпитализации в наркологический стационар. Полученные данные позволяют рассматривать аллель A1 гена DRD2 как значимый маркер риска формирования наркологического расстройства у подростков.
Ключевые слова
генетика, зависимость, подростки, наркология, психоактивные вещества, DRD2, rs1800497
Для цитирования
Панов А. С., Винникова М. А. Ассоциации полиморфизма гена DRD2 (rs1800497) с формированием наркологического заболевания в подростковом возрасте. Медицина 2026; 14(1): 36-49
DOI
Введение
В развитии наркологического заболевания участвует большое количество нейробиологических систем головного мозга и, соответственно, множество генов, ответственных за регуляцию нейрохимических процессов [1, 2]. Изучение биологических механизмов, определяющих индивидуальную уязвимость к формированию зависимости, остается одной из приоритетных задач современной наркологии.
Одним из наиболее изученных генов-кандидатов является ген DRD2, кодирующий дофаминовый рецептор второго типа. Дофаминергическая система мозга играет ключевую роль в механизмах мотивации, подкрепления и формирования патологического влечения к психоактивным веществам (ПАВ) [1, 3, 4]. Особый интерес представляет полиморфизм rs1800497 (также известный как TaqIA), локализованный в прилегающем гене ANKK1, но влияющий на экспрессию и плотность D2-рецепторов в стриатуме [1, 5]. Носительство минорного аллеля A1 (генотипы A1/A1 и A1/A2) ассоциировано со снижением плотности дофаминовых рецепторов, что может лежать в основе «синдрома дефицита вознаграждения» и повышать риск аддиктивной патологии [1, 3, 6, 7]. В исследованиях взрослых пациентов показано, что аллель A1 чаще встречается при алкогольной, опиоидной и кокаиновой зависимости, причем у носителей отмечается более раннее начало употребления и более тяжелое течение заболевания [1, 3, 8].
Подростковый возраст представляет собой критический период с точки зрения нейробиологического развития и инициации потребления ПАВ. Процессы созревания префронтальной коры и дофаминергической системы в этом возрасте создают повышенную уязвимость к аддиктивным воздействиям [1, 8]. Однако исследований, посвященных изучению роли полиморфизма rs1800497 именно в подростковой популяции, недостаточно. Имеющиеся данные свидетельствуют, что у подростков-носителей аллеля A1 для развития злоупотребления ПАВ требуется меньшее число неблагоприятных социальных факторов, что подчеркивает значительный вклад генетической предиспозиции [8].
При проведении генетических исследований важно учитывать методологические аспекты анализа. В большинстве европейских популяций частота минорного аллеля A1 составляет около 20–30%, вследствие чего гомозиготный генотип A1/A1 встречается относительно редко (в 5–10% случаев) [10]. Это ограничивает статистическую мощность при разделении выборки на три группы. Использование доминантной модели анализа (объединение носителей A1/A1 и A1/A2 в одну группу) позволяет повысить мощность и снизить вероятность ошибки II рода, что подтверждено крупными мета-анализами [7, 11]. В то же время аддитивная модель, предполагающая сравнение всех трех генотипов, дает возможность выявить возможный дозозависимый эффект аллеля A1, если таковой существует [12]. Применение обеих моделей в рамках одного исследования представляется наиболее обоснованным подходом. Учитывая сохраняющуюся потребность в идентификации генетических маркеров риска для разработки персонализированных стратегий профилактики и раннего вмешательства, изучение роли полиморфизма DRD2 (rs1800497) у подростков представляется актуальным и практически значимым.
Цели и задачи исследования
Цель исследования: Изучение ассоциации полиморфизма гена DRD2 (rs1800497) с формированием наркологической патологии у подростков.
Задачи исследования:
1) Провести анализ распределения частот генотипов и аллелей гена DRD2 (rs1800497) у подростков, употребляющих психоактивные вещества.
2) Оценить связь различных вариантов генотипа DRD2 (rs1800497) с качественными и количественными характеристиками потребления ПАВ, а также с потребностью в стационарной наркологической помощи.
Материал и методы исследования
Исследование проведено в Государственном бюджетном учреждении здравоохранения города Москвы «Московский научно-практический центр наркологии Департамента здравоохранения города Москвы» (далее – ГБУЗ «МНПЦ наркологии ДЗМ») в филиале детского наркологического диспансера. Дизайн – обсервационное одномоментное (поперечное) исследование. В исследование включались подростки в возрасте от 15 до 18 лет, проходившие обследование у врача психиатра-нарколога, а также пациенты, состоящие на диспансерном наблюдении. Набор проводился с июня 2021 по май 2023 г. Всего включено 188 подростков, средний возраст – 16,3±0,73 года; 94 юноши, 94 девушки. Критерии включения: возраст 15–18 лет, наличие информированного согласия, факт употребления психоактивных веществ (ПАВ) в анамнезе (включая эпизодическое употребление). Критерии исключения: врождённые органические поражения головного мозга; тяжёлые черепно-мозговые травмы, менингиты, энцефалиты в анамнезе; опухоли головного мозга; врождённые расстройства интеллекта; эпилепсия с детского возраста; детский тип шизофрении.
Диагнозы устанавливались врачом психиатром-наркологом по критериям МКБ-10. Распределение участников по диагнозам представлено в таблице 1. В выборку вошли как пациенты с синдромом зависимости (F19.2) и пагубным употреблением (F10.1, F19.1), так и подростки группы риска (Z72.1 – употребление алкоголя) для оценки ассоциаций генотипа с различными формами потребления ПАВ.
Таблица 1. Клиническая характеристика участников исследования
| Диагноз по МКБ-10 | Количество пациентов, абс (%) |
|---|---|
| F10.1 Психические расстройства и расстройства поведения, связанные с употреблением алкоголя. Пагубное (с вредными последствиями) употребление | 27 (14,4) |
| F19.1 Психические и поведенческие расстройства, вызванные одновременным употреблением нескольких наркотических средств и использованием других психоактивных веществ. Пагубное (с вредными последствиями) употребление | 49 (26,1) |
| F19.2 Психические и поведенческие расстройства, вызванные одновременным употреблением нескольких наркотических средств и использованием других психоактивных веществ. Синдром зависимости. В настоящее время воздержание. | 68 (36,2) |
| Z72.1 Проблемы, связанные с образом жизни. Употребление алкоголя | 44 (23,4) |
| Всего: | 188 (100) |
Клинические методы. Структурированный сбор данных проводился с использованием авторской регистрационной карты, разработанной на основе методических рекомендаций [13]. Фиксировались сведения о частоте употребления различных классов ПАВ (алкоголь, никотин, каннабиноиды, синтетические каннабиноиды, опиоиды, лекарственные вещества, кокаин, психостимуляторы, синтетические катиноны, галлюциногены, летучие органические вещества (ЛОВ)). Для количественной оценки частота употребления переводилась в баллы: «0 раз» = 0; «1–2 раза» = 1; «до 5 раз» = 2; «до 10 раз» = 3; «до 20 раз» = 4; «до 40 раз» = 5; «более 40 раз» = 6.
Молекулярно-генетические методы. ДНК выделяли из клеток буккального эпителия (образцы слюны). Генотипирование полиморфизма rs1800497 гена DRD2 проводили методом полимеразной цепной реакцией в реальном времени с аллель-специфичной гибридизацией (Real-time PCR). Условия хранения ДНК: +4 °С (до 10 дней) или –20 °С (до 1 года).
Расчёт размера выборки выполнен с использованием программы Power and Sample Size Calculations (версия 3.0.43). Исходные параметры: уровень значимости α = 0,05, мощность 80%, ожидаемый размер эффекта (разница в частоте употребления ПАВ между носителями и неносителями аллеля A1) принят равным не менее 20% на основе литературных данных [7, 10]. Расчёт показал необходимость включения не менее 170 человек.
Статистический анализ проведён с использованием программы StatTech v.4.8.5 (ООО «Статтех», Россия) [14]. Категориальные данные представлены абсолютными и относительными (%) частотами. Сравнение долей выполнено с помощью критерия χ² Пирсона; апостериорные сравнения – с поправкой Холма. Для количественных данных оценивали нормальность распределения (критерии Шапиро–Уилка или Колмогорова–Смирнова). В связи с отсутствием нормального распределения данные описаны медианой (Me) и межквартильным размахом (Q1–Q3). Сравнение двух независимых групп по количественному признаку проводили U-критерием Манна–Уитни, трёх и более групп – критерием Краскела–Уоллиса с апостериорными сравнениями по Данну (поправка Холма). Рассчитывали отношение шансов (ОШ) с 95% доверительным интервалом (ДИ). В связи с поисковым характером работы и ограниченным размером выборки коррекция на множественные сравнения не применялась; результаты рассматриваются как предварительные. Различия считали значимыми при p < 0,05.
Генетические модели анализа. Для полиморфизма rs1800497 использовали две модели: доминантную (сравнение носителей аллеля A1 – генотипы A1/A1 + A1/A2 – с гомозиготами A2/A2) и аддитивную (сравнение трёх генотипов A1/A1, A1/A2, A2/A2). Выбор моделей обоснован литературными данными о возможном доминантном и дозозависимом эффекте аллеля A1 [2, 7, 11].
Этическое обеспечение. Исследование одобрено локальным этическим комитетом ГБУЗ «МНПЦ наркологии ДЗМ» (заключение №04-21 от 12.05.2021 года). От всех участников и/или их законных представителей получено информированное согласие на участие в исследовании и обработку персональных данных.
Результаты
Учитывая характерную для подростков склонность к полисубстантному употреблению, в работе проведён анализ качественных (наличие хотя бы однократной пробы) и количественных (частота употребления, выраженная в баллах) показателей для одиннадцати классов психоактивных веществ. Детальное описание классов ПАВ и шкалы перевода частоты в баллы приведено в разделе «Материалы и методы». Далее представлены результаты сравнительного анализа показателей употребления в зависимости от генотипа DRD2 (rs1800497) согласно доминантной (A1/A1 + A1/A2 vs A2/A2) и аддитивной (A1/A1 vs A1/A2 vs A2/A2) моделям.
В исследовании частота встречаемости генотипов гена DRD2 (rs1800497) распределилась согласно Таблице 2.
Таблица 2. Частота встречаемости генотипов DRD2 (rs1800497) у подростков
| Генотип | Абс. знач. | % | 95% Доверительный интервал |
|---|---|---|---|
| A1/A1 | 13 | 7,0 | 3,7 – 11,5 |
| A1/A2 | 64 | 34,0 | 27,3 – 41,3 |
| A2/A2 | 111 | 59,0 | 51,7 – 66,1 |
При анализе по доминантной модели (A1/A1 + A1/A2 vs A2/A2) статистически значимые различия в частоте проб выявлены для шести из одиннадцати классов ПАВ: синтетических каннабиноидов, кокаина, психостимуляторов, синтетических катинонов, галлюциногенов и летучих органических веществ (Таблица 3). Во всех случаях подростки – носители аллеля A1 достоверно чаще имели опыт употребления указанных веществ по сравнению с гомозиготами A2/A2. Шансы попробовать данные виды ПАВ в группе A2/A2 были значимо ниже: от 1,8 раза для психостимуляторов до 2,6 раза для синтетических катинонов. Наиболее выраженные различия наблюдались для синтетических катинонов (ОШ = 0,390; 95% ДИ: 0,215–0,710; шансы ниже в 2,56 раза), летучих веществ (ОШ = 0,408; 95% ДИ: 0,217–0,766; шансы ниже в 2,45 раза) и галлюциногенов (ОШ = 0,432; 95% ДИ: 0,227–0,822; шансы ниже в 2,31 раза). Полные данные представлены в Таблице 3.
Таблица 3. Качественные показатели употребления ПАВ (A1/A1+A1/A2 vs A2/A2)
| Вид ПАВ | DRD2 (rs1800497) | χ2 | df | p-value | ||
|---|---|---|---|---|---|---|
| Генотип A1/A1+A1/A2, абс (%) | Генотип A2/A2, абс (%) | |||||
| Проба синтетических каннабиноидов | НЕТ | 58 (75,3) | 97 (87,4) | 4,571 | 1 | 0,033 |
| ДА | 19 (24,7) | 14 (12,6) | ||||
| Проба кокаина /«крэка» | НЕТ | 50 (64,9) | 87 (78,4) | 4,156 | 1 | 0,041 |
| ДА | 27 (35,1) | 24 (21,6) | ||||
| Проба психостимуляторов | НЕТ | 27 (35,1) | 55 (49,5) | 3,879 | 1 | 0,049 |
| ДА | 50 (64,9) | 56 (50,5) | ||||
| Проба синтетических катинонов | НЕТ | 33 (42,9) | 73 (65,8) | 9,702 | 1 | 0,002 |
| ДА | 44 (57,1) | 38 (34,2) | ||||
| Проба галлюциногенов | НЕТ | 47 (61,0) | 87 (78,4) | 6,676 | 1 | 0,010 |
| ДА | 30 (39,0) | 24 (21,6) | ||||
| Проба ЛОВ | НЕТ | 44 (57,1) | 85 (76,6) | 7,973 | 1 | 0,005 |
| ДА | 33 (42,9) | 26 (23,4) | ||||
При анализе по аддитивной модели (сравнение трёх генотипов) статистически значимые межгрупповые различия в частоте проб подтвердились для четырёх видов ПАВ (Таблица 4). Подростки с генотипом A1/A1 статистически чаще пробовали синтетические каннабиноиды, синтетические катиноны и галлюциногены по сравнению с гомозиготами A2/A2. Дозозависимый эффект аллеля A1 был выявлен для синтетических катинонов и соблюдался статистически значимым отличием по факту употребления ПАВ в линейной последовательности от группы к группе, начиная с подростков с генотипом A1/A1 – 69,2% к подросткам с генотипом A1/A2 – 54,7% и заканчивая группой подростков с генотипом A2/A2 – 34,2% (p A1/A1 – A2/A2 = 0,028; p A1/A2 – A2/A2 = 0,025). Аналогичная тенденция наблюдалась для синтетических каннабиноидов (p A1/A1 – A2/A2 = 0,043) и галлюциногенов (p A1/A1 – A2/A2 = 0,033), однако значимые различия наблюдались только между группами с гомозиготными генотипами. Носители гетерозиготного генотипа A1/A2, в свою очередь, значимо чаще имели опыт употребления синтетических катинонов и ЛОВ также относительно группы A2/A2.
Таблица 4. Качественные показатели употребления ПАВ (A1/A1 vs A1/A2 vs A2/A2)
| Вид ПАВ | DRD2 (rs1800497) | p-value | |||
|---|---|---|---|---|---|
| Генотип A1/A1, абс (%) | Генотип A1/A2, абс (%) | Генотип A2/A2, абс (%) | |||
| Проба синтетических каннабиноидов | НЕТ | 8 (61,5) | 50 (78,1) | 97 (87,4) | 0,036 pA1/A1 – A2/A2 = 0,043 |
| ДА | 5 (38,5) | 14 (21,9) | 14 (12,6) | ||
| Проба кокаина / «крэка» | НЕТ | 8 (61,5) | 42 (65,6) | 87 (78,4) | 0,120 |
| ДА | 5 (38,5) | 22 (34,4) | 24 (21,6) | ||
| Проба психостимуляторов | НЕТ | 3 (23,1) | 24 (37,5) | 55 (49,5) | 0,091 |
| ДА | 10 (76,9) | 40 (62,5) | 56 (50,5) | ||
| Проба синтетических катинонов | НЕТ | 4 (30,8) | 29 (45,3) | 73 (65,8) | 0,005 pA1/A1 – A2/A2 = 0,028 pA1/A2 – A2/A2 = 0,025 |
| ДА | 9 (69,2) | 35 (54,7) | 38 (34,2) | ||
| Проба галлюциногенов | НЕТ | 6 (46,2) | 41 (64,1) | 87 (78,4) | 0,015 pA1/A1 – A2/A2 = 0,033 |
| ДА | 7 (53,8) | 23 (35,9) | 24 (21,6) | ||
| Проба ЛОВ | НЕТ | 9 (69,2) | 35 (54,7) | 85 (76,6) | 0,011 pA1/A2 – A2/A2 = 0,008 |
| ДА | 4 (30,8) | 29 (45,3) | 26 (23,4) | ||
При анализе количественных показателей употребления (в баллах) полученные результаты согласуются с данными качественного анализа. У подростков – носителей аллеля A1 (генотипы A1/A1 + A1/A2) выявлены статистически значимо более высокие значения частоты употребления для тех же шести видов ПАВ: синтетических каннабиноидов (p = 0,025), кокаина (p = 0,026), психостимуляторов (p = 0,030), синтетических катинонов (p = 0,003), галлюциногенов (p = 0,008) и летучих органических веществ (p = 0,007) по сравнению с группой A2/A2. Данные отражены в Таблице 5, при сравнении применялся метод: U–критерий Манна–Уитни.
Таблица 5. Количественные показатели употребления ПАВ (A1/A1+A1/A2 vs A2/A2)
| Вид и частота употребления ПАВ (медиана; нижний и верхний квартили) | DRD2 (rs1800497) | U | df | p-value | ||
|---|---|---|---|---|---|---|
| Генотип A1/A1+A1/A2, баллы | Генотип A2/A2, баллы | |||||
| Синтетические каннабиноиды | Me | 0,00 | 0,00 | 3730,5 | – | 0,025 |
| Q1 – Q3 | 0,00 – 1,00 | 0,00 – 0,00 | ||||
| Кокаин/«крэк» | Me | 0,00 | 0,00 | 3635,5 | – | 0,026 |
| Q1 – Q3 | 0,00 – 2,00 | 0,00 – 0,00 | ||||
| Психостимуляторы | Me | 4,00 | 1,00 | 3519,5 | – | 0,030 |
| Q1 – Q3 | 0,00 – 6,00 | 0,00 – 5,00 | ||||
| Синтетические катиноны | Me | 2,00 | 0,00 | 3299 | – | 0,003 |
| Q1 – Q3 | 0,00 – 5,00 | 0,00 – 2,50 | ||||
| Галлюциногены | Me | 0,00 | 0,00 | 3502 | – | 0,008 |
| Q1 – Q3 | 0,00 – 2,00 | 0,00 – 0,00 | ||||
| ЛОВ | Me | 0,00 | 0,00 | 3453 | – | 0,007 |
| Q1 – Q3 | 0,00 – 2,00 | 0,00 – 0,00 | ||||
При анализе по аддитивной модели статистически значимые различия в частоте употребления подтвердились для четырёх видов ПАВ: синтетических каннабиноидов (p = 0,021), синтетических катинонов (p = 0,007), галлюциногенов (p = 0,012) и летучих органических веществ (p = 0,014) (Таблица 6; используемый метод: Критерий Краскела–Уоллиса). Подростки с генотипом A1/A1 и A1/A2 после первой пробы впоследствии чаще злоупотребляют синтетическими катинонами по сравнению с подростками, у которых генотип A2/A2, медиана и размах квартилей частоты употребления снижалась от группы подростков с генотипом A1/A1 (Me=2,00; Q1–Q3: 0,00–6,00) к группе подростков с генотипом A1/A2 (Me=1,50; Q1–Q3: 0,00–4,00) и далее к группе подростков с генотипом A2/A2 (Me=0,00; Q1–Q3: 0,00–2,50), что в частном случае подтверждает дозозависимый эффект аллеля A1 (p A1/A1 – A2/A2 = 0,046; p A1/A2 – A2/A2 = 0,046). Также подтвердились данные о том, что подростки с генотипом A1/A2 статистически значимо чаще злоупотребляют ЛОВ, но только по сравнению с подростками с генотипом A2/A2 (p A1/A2 – A2/A2 = 0,010). Интересно, что для психостимуляторов различия между генотипами не достигли статистической значимости (p = 0,060), однако медианные значения (A1/A1 = 5,00; A1/A2 = 4,00; A2/A2 = 1,00) и размах квартилей (A1/A1: 3,00–6,00; A1/A2: 0,00–6,00; A2/A2: 0,00–5,00) свидетельствуют о тенденции к более интенсивному употреблению среди носителей аллеля A1.
Таблица 6. Количественные показатели употребления ПАВ (A1/A1 vs A1/A2 vs A2/A2)
| Вид и частота употребления ПАВ (медиана; нижний и верхний квартили) | DRD2 (rs1800497) | H | df | p-value | |||
|---|---|---|---|---|---|---|---|
| Генотип A1/A1, баллы | Генотип A1/A2, баллы | Генотип A2/A2, баллы | |||||
| Синтетические каннабиноиды | Me | 0,00 | 0,00 | 0,00 | 7,705 | – | 0,021 pA2/A2 – A1/A1 = 0,032 |
| Q1 – Q3 | 0,00 – 2,00 | 0,00 – 0,00 | 0,00 – 0,00 | ||||
| Кокаин / «крэк» | Me | 0,00 | 0,00 | 0,00 | 4,977 | – | 0,083 |
| Q1 – Q3 | 0,00 – 2,00 | 0,00 – 1,25 | 0,00 – 0,00 | ||||
| Психостимуляторы | Me | 5,00 | 4,00 | 1,00 | 5,641 | – | 0,060 |
| Q1 – Q3 | 3,00 – 6,00 | 0,00 – 6,00 | 0,00 – 5,00 | ||||
| Синтетические катиноны | Me | 2,00 | 1,50 | 0,00 | 9,828 | – | 0,007 pA2/A2 – A1/A1 = 0,046 pA2/A2 – A1/A2 = 0,046 |
| Q1 – Q3 | 0,00 – 6,00 | 0,00 – 4,00 | 0,00 – 2,50 | ||||
| Галлюциногены | Me | 1,00 | 0,00 | 0,00 | 8,799 | – | 0,012 pA2/A2 – A1/A1 = 0,036 |
| Q1 – Q3 | 0,00 – 2,00 | 0,00 – 1,00 | 0,00 – 0,00 | ||||
| ЛОВ | Me | 0,00 | 0,00 | 0,00 | 8,593 | – | 0,014 pA2/A2 – A1/A2 = 0,010 |
| Q1 – Q3 | 0,00 – 1,00 | 0,00 – 2,25 | 0,00 – 0,00 | ||||
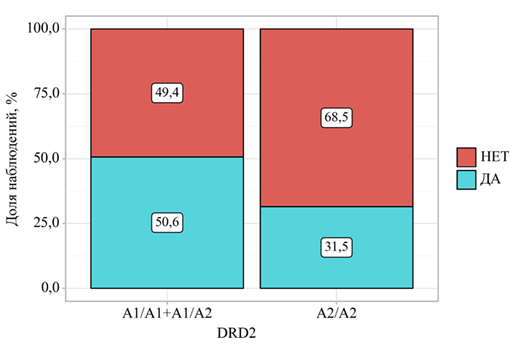
Ассоциация полиморфизма DRD2 (rs1800497) с медицинскими последствиями употребления ПАВ была также проанализирована на основании показателя госпитализации в наркологический стационар. Сравнительный анализ по доминантной модели (Рисунок 1) показал, что подростки – носители аллеля A1 (генотипы A1/A1 + A1/A2) значимо чаще нуждались в стационарном лечении по сравнению с гомозиготами A2/A2 (50,6% против 31,5%; χ² = 6,962; df = 1; p = 0,008, используемый метод: Хи-квадрат Пирсона). Шансы быть госпитализированным в группе A2/A2 оказались в 2,23 раза ниже, чем в группе носителей аллеля A1 (ОШ = 0,449; 95% ДИ: 0,246–0,818).
Рисунок 1. Сравнение частоты стационарного лечения у подростков с различными генотипами DRD2 (rs1800497): доминантная модель (A1/A1 + A1/A2 vs A2/A2)
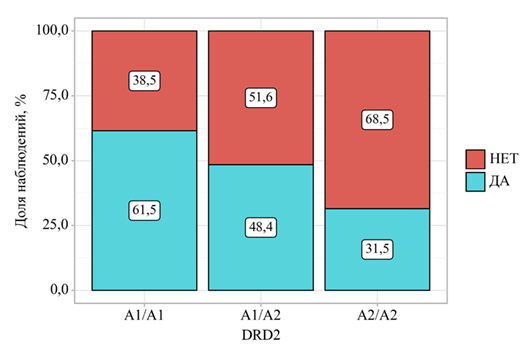
Анализ по аддитивной модели также подтвердил наличие ассоциации между генотипом DRD2 и частотой госпитализаций. Наибольшая доля подростков, проходивших стационарное лечение, наблюдалась в группе A1/A1 (61,5%), промежуточное положение занимали гетерозиготы A1/A2 (48,4%), и наименьшая частота госпитализаций зафиксирована у гомозигот A2/A2 (31,5%). Выявленные межгрупповые различия достигли статистической значимости (χ² = 7,739; df = 2; p = 0,021, используемый метод: Хи-квадрат Пирсона). Распределение частоты госпитализаций в зависимости от генотипа представлено на Рисунке 2.
Рисунок 2. Сравнение частоты стационарного лечения у подростков с различными генотипами DRD2 (rs1800497): аддитивная модель (A1/A1 vs A1/A2 vs A2/A2)
Обсуждение результатов
Полученные результаты свидетельствуют о наличии ассоциации между полиморфизмом rs1800497 гена DRD2 и особенностями потребления психоактивных веществ в подростковом возрасте. Наиболее значимые и устойчивые связи выявлены для синтетических катинонов, синтетических каннабиноидов, галлюциногенов и летучих органических веществ. Носительство аллеля A1 ассоциировано не только с более высокой вероятностью пробы данных веществ, но и с большей частотой их последующего употребления, а также с повышенной потребностью в стационарной наркологической помощи. Помимо этого, обращает на себя внимание дозозависимый эффект аллеля A1 в отношении синтетических катинонов: частота их употребления линейно возрастала от группы A2/A2 к A1/A2 и далее к A1/A1, достигая максимальных значений у гомозиготных носителей риск аллеля. Это наблюдение согласуется с данными литературы о том, что снижение плотности D2-рецепторов, наиболее выраженное именно у гомозигот A1/A1, может создавать более глубокий «дефицит вознаграждения», требующий более интенсивной стимуляции дофаминергической системы [1, 4, 15, 16]. Синтетические катиноны способны временно компенсировать этот дефицит, что может объяснять повышенное влечение к ним у генетически предрасположенных подростков [15, 17].
Интересным наблюдением стала нелинейная ассоциация аллеля A1 с употреблением летучих органических веществ: значимое повышение частоты проб и более интенсивное употребление наблюдалось у гетерозигот A1/A2, но не у гомозигот A1/A1. Это может быть связано с относительно низкой дофаминергической активностью ингалянтов по сравнению с другими ПАВ, либо с социально-демографическими факторами, характерными для подростков, употребляющих ЛОВ, которые требуют отдельного изучения.
Полученные данные согласуются с результатами более ранних исследований, демонстрирующих связь аллеля A1 с ранним началом употребления и более тяжёлым течением зависимости у взрослых [3, 8]. В то же время данное исследование дополняет картину, показывая, что генетическая предиспозиция проявляется уже в подростковом возрасте и затрагивает широкий спектр веществ, включая современные синтетические наркотики. Отсутствие значимых ассоциаций с употреблением алкоголя, никотина и каннабиноидов может объясняться высокой распространённостью этих веществ в подростковой среде, где средовые факторы (доступность, социальные нормы, групповое давление) способны нивелировать генетические различия. Для таких веществ, как психостимуляторы и кокаин, наблюдалась лишь тенденция к значимости (p = 0,060 и p = 0,083), что, вероятно, связано с недостаточной статистической мощностью и требует проверки на расширенной выборке.
Особого внимания заслуживает выявленная связь аллеля A1 с потребностью в стационарном лечении. Шансы быть госпитализированным у носителей A1 оказались в 2,23 раза выше, чем в группе A2/A2, причём максимальные показатели зафиксированы в группе A1/A1 (61,5%). Это может указывать не только на более интенсивное употребление, но и на развитие более тяжёлых форм зависимости, требующих медицинского вмешательства, что согласуется с концепцией «синдрома дефицита вознаграждения» и повышенной коморбидности у носителей риск-аллелей [2, 6, 9].
При интерпретации результатов необходимо учитывать ряд ограничений. Во-первых, относительно небольшой объём выборки (особенно малочисленность группы A1/A1) ограничивает статистическую мощность и требует подтверждения полученных закономерностей на более крупных когортах. Во-вторых, поперечный дизайн не позволяет установить явные причинно-следственные связи между генотипом и динамикой формирования зависимости. В-третьих, в связи с поисковым характером работы и отсутствием формальной коррекции на множественные сравнения (анализировалось 11 классов ПАВ), существует риск ошибки I рода. Наиболее устойчивыми и заслуживающими доверия следует считать результаты, достигшие высокого уровня значимости (p < 0,01) и подтверждённые в обеих генетических моделях, – в первую очередь для синтетических катинонов. Кроме того, исследование проводилось на выборке подростков, уже обратившихся за наркологической помощью, что ограничивает экстраполяцию выводов на общую популяцию.
Выводы
Несмотря на указанные ограничения, полученные данные свидетельствуют о значимой роли полиморфизма rs1800497 гена DRD2 как маркера повышенного риска раннего вовлечения в употребление широкого спектра ПАВ и более тяжёлого течения аддиктивного процесса у подростков. Наибольшую прогностическую ценность аллель A1 может представлять в отношении синтетических катинонов, демонстрирующих дозозависимый эффект. Дальнейшие исследования на более крупных выборках с учётом генно-средовых взаимодействий позволят уточнить возможность использования данного маркера в персонализированной профилактике и ранней диагностике наркологических расстройств в подростковой популяции.
Список литературы
1. Кибитов А.О. Генетические аспекты наркологических заболеваний: монография. 2-е изд., стереотип. М.: Прометей, 2021. 312 с.
2. Кибитов А.О., Анохина И.П. Генетические основы этиологии и патогенеза болезней зависимости от психоактивных веществ // Наркология. 2016. Т. 15, № 6 (174). С. 84–104.
3. Кибитов А.О. Молекулярно-генетический профиль дофаминовой нейромедиаторной системы при алкоголизме и героиновой наркомании: дис. ... д-ра мед. наук: 14.01.27. М., 2013. 359 с.
4. Blum K., Bowirrat A., Baron D. et al. Biotechnical development of genetic addiction risk score (GARS) and selective evidence for inclusion of polymorphic allelic risk in substance use disorder (SUD) // Journal of Systemic and Integrative Neuroscience. 2020. Vol. 6, № 2. DOI: 10.15761/JSIN.1000221.
5. Blum K., Oscar-Berman M., Barh D. et al. Dopamine Genetics and Function in Food and Substance Abuse // Journal of Genetic Syndromes & Gene Therapy. 2013. Vol. 4, № 121. DOI: 10.4172/2157-7412.1000121.
6. Chiang T.I., Lane H.Y., Lin C.H. D2 dopamine receptor gene (DRD2) Taq1A (rs1800497) affects bone density // Scientific Reports. 2020. Vol. 10. Article 13236. DOI: 10.1038/s41598-020-70262-0.
7. Blum K., Modestino E.J., Gondre-Lewis M. et al. The Benefits of Genetic Addiction Risk Score (GARS™) Testing in Substance Use Disorder (SUD) // International Journal of Genomics and Data Mining. 2018. Vol. 2018, № 1. P. 115. DOI: 10.29014/IJGD-115.000015.
8. Blum K., Bowirrat A., Elman I. et al. Evidence for the DRD2 Gene as a Determinant of Reward Deficiency Syndrome (RDS) // Clinical and Experimental Psychology. 2023. Vol. 9. P. 8–11.
9. Blum K., Thanos P.K., Hanna C. et al. «TO BE OR NOT TO BE» GWAS Ends the Controversy about the DRD2 Gene as a Determinant of Reward Deficiency Syndrome (RDS) // Psychological Research and Behavior Management. 2023. Vol. 16. P. 4287–4291. DOI: 10.2147/PRBM.S428841.
10. Noble E.P. D2 dopamine receptor gene in psychiatric and neurologic disorders and its phenotypes // American Journal of Medical Genetics Part B: Neuropsychiatric Genetics. 2003. Vol. 116B, № 1. P. 103–125. DOI: 10.1002/ajmg.b.10005.
11. Gluskin B.S., Mickey B.J. Genetic variation and dopamine D2 receptor availability: a systematic review and meta-analysis of human in vivo molecular imaging studies // Transl Psychiatry. 2016. Vol. 6, № 3. P. e747. DOI: 10.1038/tp.2016.22.
12. Blum K., Kazmi S., Modestino E.J. et al. A Novel Precision Approach to Overcome the «Addiction Pandemic» by Incorporating Genetic Addiction Risk Severity (GARS) and Dopamine Homeostasis Restoration // Journal of Personalized Medicine. 2021. Vol. 11, № 3. Article 212. DOI: 10.3390/jpm11030212.
13. Корчагина Г.А., Фадеева Е.В., Зенцова Н.И. и др. Организация мероприятий по раннему выявлению случаев употребления психоактивных веществ в образовательных учреждениях: методические рекомендации. М.: ФГБУ «ННЦ наркологии» Минздрава России, 2012. 36 с.
14. Статтех: сайт. Версия 4.8.5. URL: https://stattech.ru/ (дата обращения: 03.03.2026).
15. Асадуллин А.Р. Динамика потребления психоактивных веществ в Республике Башкортостан с углубленным клинико-генетическим изучением формирования зависимости от веществ группы синтетических катинонов: дис. ... д-ра мед. наук: 14.01.27. Уфа, 2018. 339 с.
16. Поплевченков К.Н. Персонализированный подход к терапии пациентов с зависимостью от психостимуляторов с учетом клинических, личностных и генетических факторов: автореф. дис. ... д-ра мед. наук: 3.1.17. М., 2024. 47 с.
17. Панов А.С., Винникова М.А. Влияние полиморфизма гена DRD2 на начало употребления психоактивных веществ в подростковом возрасте // Психическое здоровье: от разнообразия феноменологии к концептуальному единству: материалы Всерос. конгр. с междунар. участием (Санкт-Петербург, 22–23 мая 2025 г.) / под общ. ред. Н.Г. Незнанова. СПб.: НМИЦ ПН им. В.М. Бехтерева, 2025. С. 244–245. URL: https://disk.yandex.ru/i/5DebYZfeFuLupw (дата обращения: 03.03.2026).
Associations of the DRD2 gene polymorphism (rs1800497) with the development of substance use disorders in adolescence
Authors
Panov A. S.1
Vinnikova M. A.2
1Moscow Research & Practical Centre on Addictions of The Moscow Department of Healthcare. 109390, 37/1 Lyublinskaya street, Moscow, Russian Federation
2The State Education Institution of Higher Professional Training The First Sechenov Moscow State Medical University under Ministry of Health of the Russian Federation. 119992, 8/2, Trubetskaya street, Moscow, Russian Federation
Corresponding Author
Panov Aleksey Sergeevich; е-mail: groar@mail.ru
Conflict of interest
None declared.
Funding
The study had no sponsorship.
Received
16.03.2026
Abstract
The article presents the results of an observational cross-sectional study in the field of adolescent addiction psychiatry. It provides up-to-date information on substance use among adolescents and its association with the DRD2 gene polymorphism (rs1800497), which encodes the type 2 dopamine receptor. The study aimed to investigate the association between this genetic marker and the development of substance use disorders in adolescents. The study included 188 adolescents aged 15 to 18 years. An analysis of genotype and allele frequency distributions was conducted, and the association of the A1 allele carriage with qualitative and quantitative indicators of various classes of substance use, as well as the need for inpatient treatment, was evaluated. The results established that carriers of the A1 allele (A1/A1 and A1/A2 genotypes) were significantly more likely to try and subsequently misuse synthetic cannabinoids, synthetic cathinones, hallucinogens, and volatile organic substances compared to A2/A2 homozygotes. A dose-dependent effect of the A1 allele was identified regarding the use of synthetic cathinones. The presence of at least one A1 allele was associated with higher odds of admission to an addiction treatment hospital. The findings suggest that the A1 allele of the DRD2 gene can be considered a significant risk marker for the development of substance use disorders in adolescents.
Key words
addiction, adolescents, genetics, narcology, substance use, DRD2, rs1800497
DOI
References
1. Kibitov A.O. Geneticheskie aspekty narkologicheskikh zabolevaniy: monografiya [Genetic aspects of addictive disorders: a monograph]. 2nd ed. Moscow: Prometey, 2021. 312 p. (In Russ.)
2. Kibitov A.O., Anokhina I.P. Geneticheskie osnovy etiologii i patogeneza bolezney zavisimosti ot psikhoaktivnykh veshchestv [Genetic basis of etiology and pathogenesis of substance use disorders]. Narkologiya [Narcology]. 2016;15(6):84-104. (In Russ.)
3. Kibitov A.O. Molekulyarno-geneticheskiy profil' dofaminovoy neyromediatornoy sistemy pri alkogolizme i geroinovoy narkomanii: dis. ... d-ra med. nauk [Molecular genetic profile of the dopaminergic neurotransmitter system in alcoholism and heroin addiction: Dr. med. sci. diss.]. Moscow, 2013. 359 p. (In Russ.)
4. Blum K., Bowirrat A., Baron D. et al. Biotechnical development of genetic addiction risk score (GARS) and selective evidence for inclusion of polymorphic allelic risk in substance use disorder (SUD). Journal of Systemic and Integrative Neuroscience. 2020;6(2). DOI: 10.15761/JSIN.1000221.
5. Blum K., Oscar-Berman M., Barh D. et al. Dopamine Genetics and Function in Food and Substance Abuse. Journal of Genetic Syndromes & Gene Therapy. 2013;4(121). DOI: 10.4172/2157-7412.1000121.
6. Chiang T.I., Lane H.Y., Lin C.H. D2 dopamine receptor gene (DRD2) Taq1A (rs1800497) affects bone density. Scientific Reports. 2020;10:13236. DOI: 10.1038/s41598-020-70262-0.
7. Blum K., Modestino E.J., Gondre-Lewis M. et al. The Benefits of Genetic Addiction Risk Score (GARS™) Testing in Substance Use Disorder (SUD). International Journal of Genomics and Data Mining. 2018;2018(1):115. DOI: 10.29014/IJGD-115.000015.
8. Blum K., Bowirrat A., Elman I. et al. Evidence for the DRD2 Gene as a Determinant of Reward Deficiency Syndrome (RDS). Clinical and Experimental Psychology. 2023;9:8-11.
9. Blum K., Thanos P.K., Hanna C. et al. «TO BE OR NOT TO BE» GWAS Ends the Controversy about the DRD2 Gene as a Determinant of Reward Deficiency Syndrome (RDS). Psychological Research and Behavior Management. 2023;16:4287-4291. DOI: 10.2147/PRBM.S428841.
10. Noble E.P. D2 dopamine receptor gene in psychiatric and neurologic disorders and its phenotypes. American Journal of Medical Genetics Part B: Neuropsychiatric Genetics. 2003;116B(1):103-125. DOI: 10.1002/ajmg.b.10005.
11. Gluskin B.S., Mickey B.J. Genetic variation and dopamine D2 receptor availability: a systematic review and meta-analysis of human in vivo molecular imaging studies. Transl Psychiatry. 2016;6(3):e747. DOI: 10.1038/tp.2016.22.
12. Blum K., Kazmi S., Modestino E.J. et al. A Novel Precision Approach to Overcome the «Addiction Pandemic» by Incorporating Genetic Addiction Risk Severity (GARS) and Dopamine Homeostasis Restoration. Journal of Personalized Medicine. 2021;11(3):212. DOI: 10.3390/jpm11030212.
13. Korchagina G.A., Fadeeva E.V., Zentsova N.I. et al. Organizatsiya meropriyatiy po rannemu vyyavleniyu sluchaev upotrebleniya psikhoaktivnykh veshchestv v obrazovatel'nykh uchrezhdeniyakh: metodicheskie rekomendatsii [Organization of early detection of psychoactive substance use in educational institutions: guidelines]. Moscow: FSBI «NSC of Narcology» of the Ministry of Health of Russia, 2012. 36 p. (In Russ.)
14. Stattekh: sait [Stattech: website]. Version 4.8.5. Available at: https://stattech.ru/ (accessed 03.03.2026). (In Russ.)
15. Asadullin A.R. Dinamika potrebleniya psikhoaktivnykh veshchestv v Respublike Bashkortostan s uglublennym kliniko-geneticheskim izucheniem formirovaniya zavisimosti ot veshchestv gruppy sinteticheskikh katinonov: dis. ... d-ra med. nauk [Dynamics of psychoactive substance use in the Republic of Bashkortostan with an in-depth clinical and genetic study of the formation of dependence on synthetic cathinones: Dr. med. sci. diss.]. Ufa, 2018. 339 p. (In Russ.)
16. Poplevchenkov K.N. Personalizirovannyy podkhod k terapii patsientov s zavisimost'yu ot psikhostimulyatorov s uchetom klinicheskikh, lichnostnykh i geneticheskikh faktorov: avtoref. dis. ... d-ra med. nauk [Personalized approach to the treatment of patients with psychostimulant dependence considering clinical, personal and genetic factors: Dr. med. sci. abstr.]. Moscow, 2024. 47 p. (In Russ.)
17. Panov A.S., Vinnikova M.A. Vliyanie polimorfizma gena DRD2 na nachalo upotrebleniya psikhoaktivnykh veshchestv v podrostkovom vozraste [Influence of the DRD2 gene polymorphism on the onset of psychoactive substance use in adolescence]. In: Neznanov N.G., ed. Psikhicheskoe zdorov'e: ot raznoobraziya fenomenologii k kontseptual'nomu edinstvu: materialy Vseros. kongr. s mezhdunar. uchastiem (Sankt-Peterburg, 22–23 maya 2025 g.) [Mental health: from diversity of phenomenology to conceptual unity: proceedings of the All-Russian Congress with international participation (St. Petersburg, May 22–23, 2025)]. St. Petersburg: V.M. Bekhterev NMRC PN, 2025. P. 244-245. Available at: https://disk.yandex.ru/i/5DebYZfeFuLupw (accessed 03.03.2026). (In Russ.)