Авторы
Розенфельд И. И.
к.м.н., врач-хирург1
Чиликина Д. Л.
студентка, педиатрический факультет1
1ФГБОУ ВО «Тверской государственный медицинский университет» Минздрава России, г. Тверь, Российская Федерация
Автор для корреспонденции
Розенфельд Игорь Игоревич; e-mail: iiggo@mail.ru
Финансирование
Исследование не имело спонсорской поддержки.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Аннотация
Данная статья является продолжением цикла исследований по вопросам оптимизации техники и методики проведения хирургических операций при грыжах пищеводного отверстия диафрагмы и основывается на использовании разработки автора – модели двухслойного биокарбонового сетчатого имплантата. Целью данного исследования является освещение непосредственных и отдалённых результатов использования двухслойного биокарбонового сетчатого имплантата в сравнении со стандартной методикой использования полипропиленового имплантата при оперировании больных с большими и гигантскими грыжами пищеводного отверстия диафрагмы. Все пациенты были разделены на 2 исследовательские группы, которым была выполнена аллопластика различными имплантатами: I группа из 221 пациента, которым была выполнена аллопластика полипропиленовым сетчатым имплантатом (171 пациент с большими грыжами площадью 10-20 см2 и 50 пациентов с гигантскими грыжами пищеводного отверстия диафрагмы с площадью грыжевого дефекта более 20 см2); II группа из 79 пациентов, которым была выполнена оригинальная аллопластика двухслойным биокарбоновым сетчатым имплантатом (50 пациентов с большими грыжами и 29 пациентов с гигантскими грыжами пищеводного отверстия). Послеоперационные осложнения классифицировались по шкале «Clavien-Dindo». Индекс «De Meester» использовался в качестве критерия сравнения. В статье рассмотрены результаты операций 300 пациентов по поводу больших и гигантских грыж пищеводного отверстия диафрагмы, из которых 79 были прооперированны с использованием опытного образца биокарбонового двухслойного сетчатого имплантата по патенту автора. В работе представлены непосредственные и отдалённые результаты. Результаты хирургического лечения являются пилотными и репрезентативными, которые определяют дальнейшую тактику и направление совершенствования операций по удалению больших и гигантских грыж пищеводного отверстия диафрагмы. Впервые приведены данные по использованию авторской разработки двухслойного биокарбонового сетчатого имплантата и проведено сравнение с полипропиленовым сетчатым имплантатом при проведении «оnlay» пластики больших и гигантских грыж пищеводного отверстия диафрагмы. Получены достоверные отличия по рецидивам всех видов в пользу биокарбоновым сетчатым имплантатом (5,6 против 22,8%; р < 0,0001; точный критерий Фишера).
Ключевые слова
большие грыжи пищеводного отверстия диафрагмы, гигантские грыжи пищеводного отверстия диафрагмы, аллопластика, «оnlay» пластика, биокарбоновым двухслойным сетчатый имплантат, полипропиленовый сетчатый имплантат, техника операции
Для цитирования
Розенфельд И. И., Чиликина Д. Л. Сравнение эффективности «оnlay» пластики больших и гигантских грыж пищеводного отверстия диафрагмы полипропиленовым сетчатым имплантатом и двухслойным биокарбоновым сетчатым имплантатом. Медицина 2021; 9(1): 93-102.
DOI
Введение
Данная статья является продолжением цикла исследований по вопросам оптимизации техники и методики проведения хирургических операций при грыжах пищеводного отверстия и основывается на использовании разработки автора – модели двухслойного биокарбонового сетчатого имплантата [2,3,4].
Целью данного исследования является освещение непосредственных и отдалённых результатов использования двухслойного биокарбонового сетчатого имплантата в сравнении со стандартной методикой использования полипропиленового имплантата при оперировании больных с большими и гигантскими грыжами пищеводного отверстия диафрагмы.
Классическая методика "onlay" пластики полипропиленовым имплантатом предусматривает использование стандартной или облегчённой сетки с фиксацией её поверх сшитых ножек диафрагмы [1,6,7,9]. При этом формируется грубая рубцовая ткань, происходит значительное сморщивание сетки, сохраняется контакт имплантата с пищеводом, который приводит к развитию анатомического рецидива [5,8].
Разработанная методика лапароскопической двухслойной пластики с использованием двухслойного биокарбонового сетчатого имплантата имеет два ключевых преимущества.
Во-первых, используемый имплантат не только является облегчённым, но и частично состоит из волокон биокарбона, которые являются сверхпрочным материалом, что снижает вероятность рецидива, а также моноакрила, который рассасывается на протяжении нескольких месяцев. При этом вокруг имплантата формируется мягкая рубцовая ткань, и сморщивание сетки происходит в небольшой степени.
Во-вторых, сетчатый имплантат закрывается ножками диафрагмы, которые препятствуют его контакту с пищеводом. Таким образом, имплантат не вызывает "пилящего" эффекта при дыхательных движениях диафрагмы. Эти преимущества резко снижают риск пищеводных осложнений.
Материал и методы исследования
Всего с 2014 по 2018 год по поводу больших и гигантских грыж пищеводного отверстия диафрагмы было прооперированно 300 пациентов. Из 300 пациентов 221 была установлена полипропиленовая сетка, а 79 больных были прооперированы с использованием опытного образца двухслойного биокарбонового сетчатого имплантата по патенту автора (регистрационный № 20181 от 16.07.2018 года).
Все пациенты были разделены на 2 исследовательские группы, которым была выполнена аллопластика различными имплантатами:
● I группа из 221 пациента, которым была выполнена аллопластика полипропиленовым сетчатым имплантатом (171 пациент с большими грыжами площадью 10-20 см2 и 50 пациентов с гигантскими грыжами пищеводного отверстия диафрагмы с площадью грыжевого дефекта более 20 см2).
● II группа из 79 пациентов, которым была выполнена оригинальная аллопластика двухслойным биокарбоновым сетчатым имплантатом (50 пациентов с большими грыжами и 29 пациентов с гигантскими грыжами пищеводного отверстия).
Послеоперационные осложнения классифицировались по шкале "Clavien-Dindo", согласно которой:
● I степень – любые отклонения от нормального послеоперационного течения, которые не требуют медикаментозного лечения (кроме антипиретиков, анальгетиков, антиэметиков) или хирургического вмешательства;
● II степень – осложнения, которые не угрожают жизни, которые требует медикаментозного лечения, включая гемотрансфузии и парентеральное питание;
● III степень – осложнения, которые не угрожают жизни и требуют хирургического, эндоскопического или радиологического вмешательства:
● III а степень – без общей анестезии, III b степень – под общей анестезией;
● IV степень – осложнения, угрожающие жизни, в том числе цереброваскулярные осложнения, которые требуют лечения в условиях отделения интенсивной терапии:
● IV а степень – дисфункция одного органа, включая диализ, IV b степень – полиорганная недостаточность;
● V степень – смерть.
Индекс "De Meester" использовался в качестве критерия сравнения, в норме он равен 14,7.
Результаты исследования и их обсуждение
Непосредственные результаты
Интраоперационных осложнений в I группе не наблюдалось.
Во II группе имело место 2 случая (2,5%) пневмоторакса, который требовал дренирования плевральной полости.
Достоверных отличий по частоте интраоперационных осложнений между группами не было (0,0 против 2,5% соответственно, p=0,0643, точный критерий Фишера).
Послеоперационные осложнения в I группе имели место у 5 пациентов (2,2%): 3 случая ателектазов с лихорадкой и 1 случай инфицирования троакарной раны. Данные случаи были отнесены ко II степени по классификации "Clavien-Dindo". Также наблюдался 1 случай поддиафрагмальной гематомы, которая требовала пункционного дренирования, что относилось к III а степени по классификации "Clavien-Dindo".
Послеоперационные осложнения во II группе имели место у 2 пациентов (2,5%): ателектазы с лихорадкой, которые относились ко II степени по классификации "Clavien-Dindo".
Достоверных отличий по частоте послеоперационных осложнений между группами не было (2,2 против 2,5%, p=0,5692, точный критерий Фишера). Средний послеоперационный койко-день составил 5,7±1,7 (2–13) дней в I группы и 5,9±1,3 (от 3 до 9) дней в II группе. По послеоперационным койко-дням достоверных отличий между группами выявлено не было (5,7±1,7 против 5,9±1,3, p=0,4113, критерий Манна-Уитни) (таблица 1).
Таблица 1. Сравнение непосредственных результатов между I и II группой
| Показатель | I группа (n=221) | II группа (n=79) | Значение р |
| Интраоперационные осложнения | 2 (2,5%) | 0 | 0,0643 |
| Послеоперационные осложнения | 5 (2,2%) | 2 (2,5%) | 0,5692 |
| Послеоперационный койко-день | 5,7 ± 1,7 (2–13) | 5,9 ± 1,3 (3–9) | 0,4113 |
Отдалённые результаты
В I группе из 221 пациента анатомические рецидивы всех видов были выявлены у 13 больных (5,6%). Они были распределены следующим образом: симптомный анатомический рецидив и функциональный рецидив были выявлены у 7 пациентов (3%), симптомный анатомический рецидив – у 5 пациентов (2,2%), бессимптомный анатомический рецидив и функциональный рецидив отсутствовали, бессимптомный анатомический рецидив выявлен у 1 пациента (0,4%). Функциональные рецидивы всех видов были выявлены у 6 пациентов (2,6%). Из них симптомные функциональные рецидивы были выявлены у 5 пациентов (2,2%), бессимптомный функциональный рецидив – у 1 пациента (0,4%). Рефлюкс-эзофагит был выявлен у 10 пациентов (4,3%). Средний индекс "De Meester", измеренный у 162 пациентов, составил 15,7±25,8 (3,3–45,4). Длительная функциональная дисфагия имела место у 19 пациентов (8,2%). Стриктуры имели место в 3-х случаях (1,3%). Повторные операции выполнены 2 пациентам (0,9%): у обоих по поводу симптомного анатомического рецидива и функционального рецидива.
Во II группе из 79 пациентов анатомические рецидивы всех видов были выявлены у 18 пациентов (22,8%). Они были распределены следующим образом: симптомный анатомический рецидив и функциональный рецидив выявлены у 6 пациентов (7,6%), симптомный анатомический рецидив – у 9 пациентов (11,4%), бессимптомный анатомический рецидив и функциональный рецидив – у 1 пациентки (1,3%), бессимптомный анатомический рецидив – у 2 пациентов (2,5%). Функциональные рецидивы всех видов были выявлены у 4-х пациентов (5%). Из них симптомные функциональные рецидивы были выявлены у 3-х пациентов (3,8%), бессимптомный функциональный рецидив – у 1 пациента (1,3%). Рефлюкс- эзофагит был выявлен у 9 пациентов (11,4%). Средний индекс "De Meester", измеренный у 60 пациентов, составил 31,3±51,8 (4,1–88,5). Длительная функциональная дисфагия имела место у 7 пациентов (8,8%). Стриктура имела место в 1 случае (1,3%). Повторные операции были выполнены у 4 пациентов (5%): у 2-х пациентов по поводу симптомного анатомического рецидива и функционального рецидива, у 1 пациентки по поводу стриктуры и у 1 больного по поводу симптомного анатомического рецидива.
По частоте анатомических рецидивов всех видов было выявлено достоверное различие в пользу I группы (5,6 против 22,8%, р<0,0001, критерий х2). По частоте симптомного анатомического рецидива и функционального рецидива достоверного различия выявлено не было (3 против 7%, р=0,0806, критерий х2). По частоте симптомного анатомического рецидива выявлено достоверное различие в пользу I группы (2,2 против 11,4%, р=0,0007, критерий х2). По частоте бессимптомных анатомических рецидивов и функциональных рецидивов достоверное различие выявлено не было (0,0 против 1,3%, р=0,2548, точный критерий Фишера). По частоте бессимптомных анатомических рецидивов достоверного различия также выявлено не было (0,4 против 2,5%, р=0,1608, точный критерий Фишера). По частоте функциональных рецидивов всех видов достоверное различие выявлено не было (2,6 против 5,0%, р=0,2328, точный критерий Фишера). По частоте симптоматических функциональных рецидивов достоверного различия выявлено не было (2,2 против 3,8%, р=0,3327, точный критерий Фишера). По частоте бессимптомных функциональных рецидивов достоверное различие выявлено также не было (0,4 против 1,3%, р=0,4455, точный критерий Фишера). По частоте рефлюкс-эзофагита выявлено достоверное различие в пользу I группы (4,3 против 11,4%, р=0,0239, критерий х2). По среднему индексу "De Meester" достоверное различие выявлено не было (15,7±25,8 против 31,3±51,8, р=0,0664, критерий Манна-Уитни). По частоте длительной функциональной дисфагии достоверное различие выявлено не было (8,2 против 8,8%, р=0,8603, точный критерий Фишера). По частоте стриктур пищевода достоверное различие выявлено также не было (1,3 против 1,3%, р=0,7307, точный критерий Фишера). По частоте повторных операций выявлено достоверное различие в пользу I группы (0,9 против 5,0%, р=0,0387, точный критерий Фишера) (табл. 2).
Таблица 2. Сравнение отдалённых результатов между I и II группой
| Показатель | I группа (n = 221) | II группа (n = 79) | Значение р |
| Анатомические рецидивы всех видов | 13 (5,6%) | 18 (22,8%) | < 0,0001 |
| Симптомный анатомический рецидив и функциональный рецидив | 7 (3,0%) | 6 (7,6%) | 0,0806 |
| Симптомный анатомический рецидив | 5 (2,2%) | 9 (11,4%) | 0,0007 |
| Бессимптомный анатомический рецидив и функциональный рецидив | 0 (0,0%) | 1 (1,3%) | 0,2548 |
| Бессимптомный анатомический рецидив | 1 (0,4%) | 2 (2,5%) | 0,1608 |
| Функциональный рецидив всех видов | 6 (2,6%) | 4 (5,0%) | 0,2328 |
| Симптомные функциональные рецидивы | 5 (2,2%) | 3 (3,8%) | 0,3327 |
| Бессимптомный функциональный рецидив | 1 (0,4%) | 1 (1,3%) | 0,4455 |
| Рефлюкс – эзофагит | 10 (4,3%) | 9 (11,4%) | 0,0239 |
| Индекс "De Meester" | 15,7 ± 25,8 (3,3–45,4) | 31,3 ± 51,8 (4,1–88,5) | 0,0664 |
| Длительная функциональная дисфагия | 19 (8,2%) | 7 (8,8%) | 0,8603 |
| Стриктуры пищевода | 3 (1,4%) | 1 (1,3%) | 0,7307 |
| Повторные операции | 2 (0,9%) | 4 (5,0%) | 0,0387 |
На основе анализа показателей рецидивов с использованием полипропиленового и биокарбонового имплантата была предложена методика двухслойной пластики, которую рекомендовалось выполнять по разработанной методике. Сначала мобилизовались ножки диафрагмы и части желудка, которая мигрировала, с удалением грыжевого мешка и созданием позадипищеводного туннеля, мобилизация дна желудка путём частичного рассечения желудочно-селезёночной связки и мобилизация пищевода с устранением его укорочения путём параэзофагеальной медиастинальной диссекции. Потом следует выполнить собственно пластику. Сначала края двухслойного биокарбонового сетчатого имплантата в форме равнобедренного треугольника с длиной сторон по 4 см и длиной основания 3 см должны фиксироваться к каждой из ножек диафрагмы позади пищевода 2–3 узловыми нерассасывающимися швами (рис. 1).
Рис. 1. Фиксация имплантата к ножкам диафрагмы
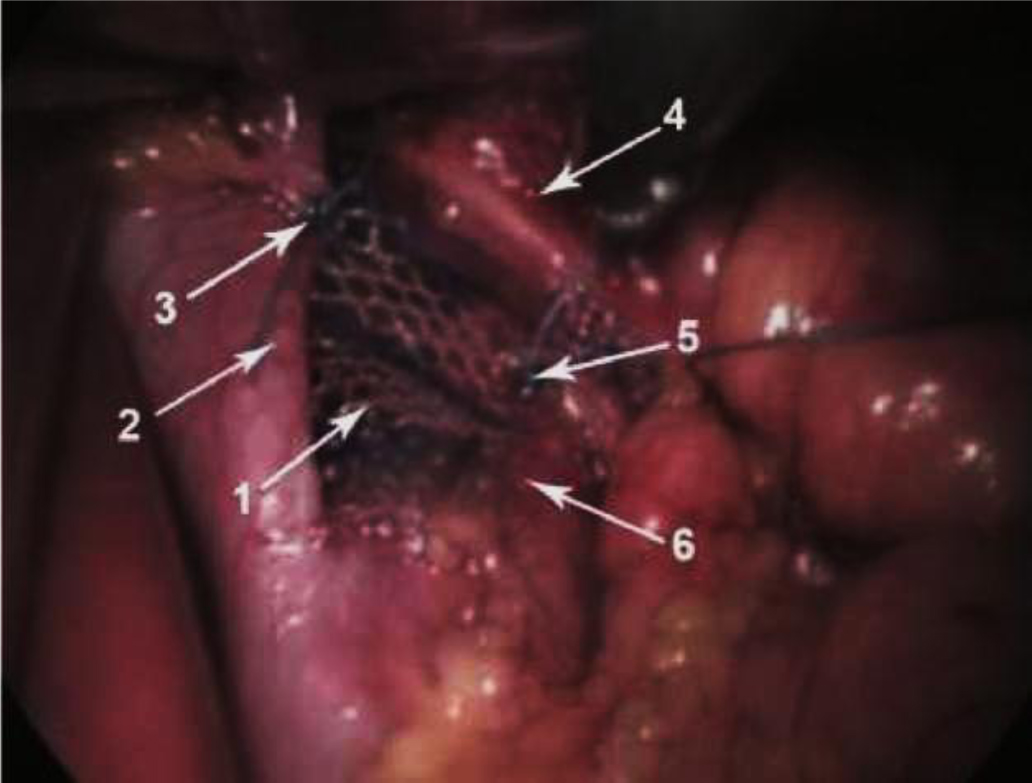
1 – сетчатый имплантат; 2 – правая ножка диафрагмы; 3 – шов, фиксирующий имплантат к правой ножки диафрагмы; 4 – пищевод; 5 – шов, фиксирующий имплантат к левой ножке диафрагмы; 6 – левая ножка диафрагмы.
При этом верхний край имплантата в виде основания треугольника не должен доходить до пищевода, полностью поднятого кверху на 1 см для исключения контакта. Таким образом, будет создаваться "первый пласт". Потом 2-3 узловыми швами ножки диафрагмы сшиваются между собой, что приводит к полному закрытию имплантата (рис. 2).
Рис. 2. Сшивание ножек с закрытием имплантата
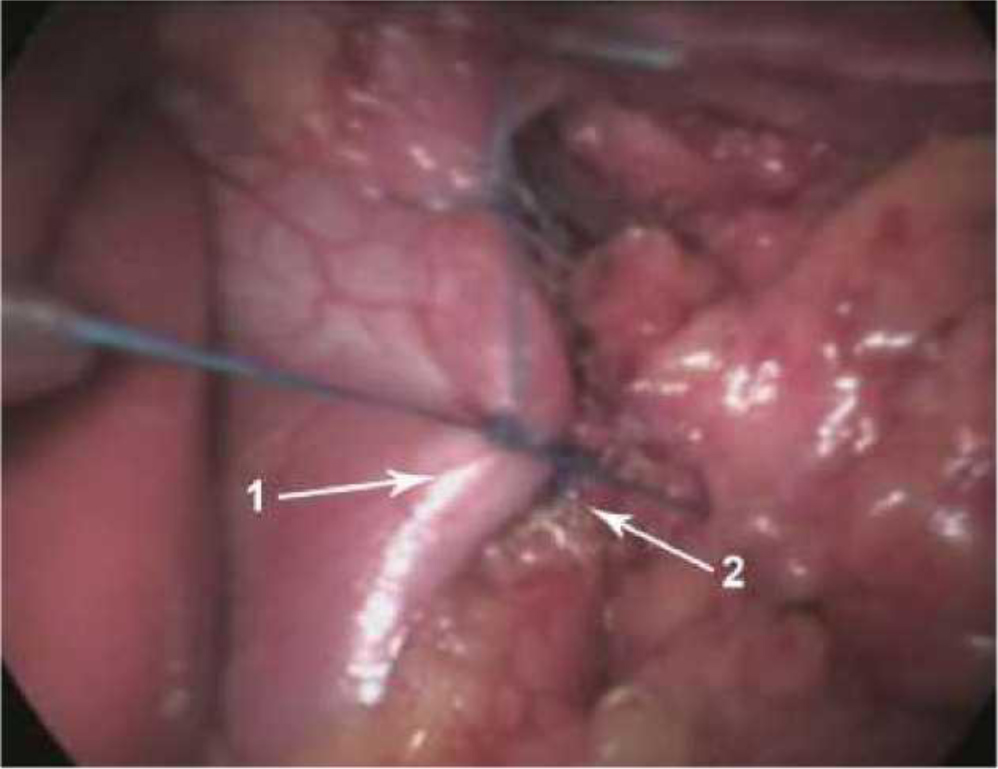
1 – правая ножка диафрагмы; 2 – левая ножка диафрагмы.
При этом верхний шов не должен доходить до пищевода, полностью поднятого кверху на 0,5-1 см. Таким образом, будет создаваться "второй пласт". Пластику следует выполнять при введённом в желудок калибровочном зонде диаметром 30 Fr. Следующий этап – фундопликация по Ниссену с длиной манжетки 3 см, а также нерассасывающимся шовным материалом с использованием калибровочного зонда.
Выводы
По частоте анатомических рецидивов, в частности симптомных анатомических рецидивов, аллопластика дала достоверно худшие результаты во II исследовательской группе.
Аналогичные результаты были получены по частоте рефлюкс – эзофагита и повторным операциям. Достоверных отличий между сравниваемыми группами по частоте анатомических рецидивов выявлено не было.
Результаты аллопластики в II группе при использовании биокарбонового имплантата можно считать близкими к удовлетворительным, но они требуют улучшения за счёт использования особой техники проведения операций.
Результаты использования данной методики проведения операций будут статистически сравнены в дальнейших публикациях автора.
Список литературы
1. Грубник В.В., Малиновский А.В. Критические аспекты лапароскопической хирургии гастроэзофагеальной рефлюксной болезни и гриж пищеводного отверстия диафрагмы. Одесса: ВМВ-типография, 2015. 106 с.
2. Розенфельд И.И., Акопян В.А. Классификация негативных результатов лапароскопических операций при грыжах пищеводного отверстия диафрагмы. Материалы XII Международной научно-практической конференции студентов и молодых учёных-медиков «Молодежь – практическому здравоохранению». Тверь: ФГБОУ ВО Тверской ГМУ Минздрава России. Совет молодых учёных и студентов. 2018; 856-858.
3. Розенфельд И.И., Чиликина Д.Л. Оценка результатов использования сетчатых имплантатов при аллопластике грыж пищеводного отверстия диафрагмы. Исследование и практика в медицине. 2018; 5 (4): 156-158.
4. Розенфельд И.И., Чиликина Д.Л. Проблема больших и гигантских грыж пищеводного отверстия диафрагмы и результаты основных методов их пластики. Анналы хирургии. 2018; 3: 74-79.
5. Antoniou S.A., Koch O.O., Antoniou G.A. Mesh-reinforced hiatal hernia repair: a review on the effect on postoperative dysphagia and recurrence. Langenbeck's archives of surgery. 2012; 397 (1): 19-27. doi: 10.1007/s00423-011-0829-0
6. Frantzides C.T., Carlson M.A., Loizides S. Hiatal hernia repair with mesh: a survey of SAGES members. Surgical endoscopy. 2010; 24 (5): 1017-24. doi: 10.1007/s00464-009-0718-6
7. Furnée E., Hazebroek E Mesh in laparoscopic large hiatal hernia repair: a systematic review of the literature. Surgical endoscopy. 2013; 27 (11): 3998-4008. doi: 10.1007/s00464-013-3036-y
8. Granderath F.A., Schweiger U.M., Kamolz T. Laparoscopic antireflux surgery with routine mesh-hiatoplasty in the treatment of gastroesophageal reflux disease. Journal of gastrointestinal surgery. 2002; 6 (3): 347-353. doi: 10.1016/s1091-255x(01)00025-7
9. Targarona E.M., Grisales S., Uyanik O. Long-term outcome and quality of life after laparoscopic treatment of large paraesophageal hernia. World journal of surgery. 2013; 37 (8): 1878–1882. doi: 10.1007/s00268-013-2047-0
Comparison of the Effectiveness of «Оnlay» Plastics of Large and Giant Hernias of The Esophageal Aperture of the Diaphragm with a Polypropylene Mesh Implant and a Biocarbon Double-Layer Mesh Implant
Authors
Rozenfeld I. I.
MD PhD1
Chilikina D. L.
Student, Pediatric Faculty1
1Tver State Medical University, Tver, Russia
Corresponding Author
Rozenfeld Igor; e-mail: iiggo@mail.ru
Conflict of interest
None declared.
Funding
The study had no sponsorship.
Abstract
This article is a continuation of a series of studies on the optimization of techniques and methods of surgical operations for hernias of the esophageal aperture of the diaphragm and is based on the use of the author’s development of a model of a two-layer biocarbon mesh implant. The purpose of this study is to highlight the immediate and long-term results of using a double-layer biocarbon mesh implant in comparison with the standard method of using a polypropylene implant when operating patients with large and giant hiatal hernia. All patients were split into 2 research groups that underwent alloplasty with various implants: Group I of 221 patients who underwent alloplasty with a polypropylene mesh implant (171 patients with large hernias of 10-20 cm2) and 50 patients with giant hernias of the esophageal orifice with the area of the hernial defect exceeding 20 cm2); Group II of 79 patients who underwent an original alloplasty with a bi-layer biocarbon mesh implant (50 patients with large hernias and 29 patients with giant hernia of the esophageal orifice). Postoperative complications were classified according to the Clavien-Dindo scale. De Meester index was used as a comparison criterion. The article discusses the results of operations of 300 patients for large and giant hernias of the esophageal aperture of the diaphragm, of which 79 were operated on using a prototype biocarbon double-layer mesh implant according to the author's patent. The paper presents immediate and long-term results. The results of surgical treatment are pilot and representative, which determine the further tactics and direction of improving operations to remove large and giant hernias of the esophageal opening of the diaphragm. For the first time, data on the use of the author's development of a bi-layer biocarbon mesh implant are presented and compared with a polypropylene mesh implant during an «on-line» plastic repair of large and giant hiatal hernia. Significant differences were obtained in relapses of all types in favor of a biocarbon mesh implant (5,6 versus 22,8%; p < 0,0001; Fisher's exact test).
Key words
large hernias of the esophageal aperture of the diaphragm, giant hernias of the esophageal aperture of the diaphragm, alloplasty, «onlay» plastic, biocarbon double-layer mesh implant, polypropylene mesh implant, surgery technique
DOI
References
1. Grubnik V.V., Malinovskij A.V. Kriticheskie aspekty laparoskopicheskoj hirurgii gastroezofageal'noj reflyuksnoj bolezni i grizh pishchevodnogo otverstiya diafragmy. [Critical aspects of laparoscopic surgery of gastroesophageal reflux disease and esophageal cavity.]« Odessa. VMV-tipografiya. 2015: 106 p. (In Russ.)
2. Rozenfel’d I.I., Akopyan V.A. Klassifikaciya negativny`h rezul`tatov laparoskopicheskih operacij pri gry`zhah pishhevodnogo otverstiya diafragmy. [Classification of negative results of laparoscopic operations for hiatal hernia]. Proceedings of the XII International Scientific and Practical Conference of Students and Young Medical Scientists »Youth for Practical Health Care«. Tver: FSBEI of Tver State Medical University of the Ministry of Health of Russia. Council of Young Scientists and Students. 2018; 856-858. (In Russ.)
3. Rozenfel`d I.I., Chilikina D.L. Ocenka rezul`tatov ispol`zovaniya setchaty`h implantatov pri alloplastike gry`zh pishhevodnogo otverstiya diafragmy [Assessment of the results of using mesh implants in alloplasty of the hiatal hernia.] Issledovanie i praktika v medicine [Research and practice in medicine] 2018; 5 (4): 156-158. (In Russ.)
4. Rozenfel`d I.I., Chilikina D.L. Problema bol`shix i gigantskix gry`zh pishhevodnogo otverstiya diafragmy` i rezul`taty` osnovny`x metodov ix plastiki. [The problem of large and giant hiatal hernia and the results of the main methods of plastics.] Annaly` xirurgii [Annals of Surgery] 2018; 3: 74-79. (In Russ.)
5. Antoniou S.A., Koch O.O., Antoniou G.A. Mesh-reinforced hiatal hernia repair: a review on the effect on postoperative dysphagia and recurrence. Langenbeck's archives of surgery. 2012; 397 (1): 19-27. doi: 10.1007/s00423-011-0829-0
6. Frantzides C.T., Carlson M.A., Loizides S. Hiatal hernia repair with mesh: a survey of SAGES members. Surgical endoscopy. 2010; 24 (5): 1017-24. doi: 10.1007/s00464-009-0718-6
7. Furnée E., Hazebroek E. Mesh in laparoscopic large hiatal hernia repair: a systematic review of the literature. Surgical endoscopy. 2013; 27 (11): 3998-4008. doi: 10.1007/s00464-013-3036-y
8. Granderath F.A., Schweiger U.M., Kamolz T. Laparoscopic antireflux surgery with routine mesh-hiatoplasty in the treatment of gastroesophageal reflux disease. Journal of gastrointestinal surgery. 2002; 6 (3): 347-353. doi: 10.1016/s1091-255x(01)00025-7
9. Targarona E.M., Grisales S., Uyanik O. Long-term outcome and quality of life after laparoscopic treatment of large paraesophageal hernia. World journal of surgery. 2013; 37 (8): 1878-1882. doi: 10.1007/s00268-013-2047-0
