| О журнале | Редколлегия | Редсовет | Архив номеров | Поиск | Авторам | Рецензентам | English |
Изучение метаболического профиля каннабимиметика MDMB-2201 в моче методом газовой хроматографии с масс-спектрометрическим детектированием
Автор для корреспонденции: Дворская Оксана Николаевна, e-mail: dvoksnik@gmail.com. Финансирование. Исследование не имело спонсорской поддержки. Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов. Аннотация Первые случаи выявления потребителей каннабимиметика MDMB-2201 при исследовании мочи на наркотические вещества в Российской Федерации произошли в марте-апреле 2019 года в городах Тюмень, Екатеринбург, Курган. В моче потребителей курительных смесей с использованием твердофазной экстракции и газовой хроматографии с масс-спектрометрическим детектированием выявлены 15 основных метаболитов и маркеров каннабимиметика MDMB-2201. Получены масс-спектры электронной ионизации выявленных метаболитов MDMB-2201, результаты расчетов ряда физико-химических характеристик и степени конъюгации метаболитов для установления фактов приема каннабимиметика MDMB-2201 при анализе изъятых биообъектов. Ключевые слова MDMB-2201, каннабимиметики, метаболиты, моча, твердофазная экстракция, газовая хроматография - масс-спектрометрия doi: 10.29234/2308-9113-2019-7-3-104-120 Для цитирования: Катаев С. С., Дворская О. Н., Гофенберг М. А., Дунилин А. В. Изучение метаболического профиля каннабимиметика MDMB-2201 в моче методом газовой хроматографии с масс-спектрометрическим детектированием. Медицина 2019; 7(3): 104-120 Введение Многие синтетические каннабимиметики, синтезированные в научных целях при поиске новых лекарственных средств, стали предметом неправомерного использования в качестве наркотических средств, способствуя, таким образом, расширению номенклатуры нелегальных веществ на рынке незаконного оборота наркотиков. В ноябре 2016 года в Бельгии с использованием различных аналитических прикладных методов был идентифицирован новый каннабимиметик 5F-MDMB-PICA (MDMB-2201) в образцах порошка и "спайсов", поступивших в лабораторию на токсикологическое исследование [8]. С фармакологической точки зрения MDMB-2201 является мощным высокоэффективным агонистом каннабиноидных рецепторов (CB1 EC50 = 0.45 нМ; CB2 EC50 = 7.4 нМ) с преимущественной активацией рецепторов 1-го типа [4]. В работе Mogler с соавторами [7] представлены результаты исследования метаболизма MDMB-2201 in vivo на гепатоцитах печени человека и in vivo в моче потребителей с использованием ЖХ-МС/МС. Первые случаи выявления потребителей каннабимиметика MDMB-2201 при исследовании мочи на наркотические вещества в Российской Федерации произошли в марте и апреле 2019 года в городах Тюмень, Екатеринбург, Курган. Каннабимиметик MDMB-2201, как производное метилового эфира 3-метил-2-(1-пентил-1H-индол-3-карбоксамидо) бутановой кислоты, отнесен к I Списку Постановления Правительства РФ № 578 от 23.06.2014 [3]. MDMB-2201 является аналогом известного соединения MDMB(N)-2201 [4-6] и отличается от последнего наличием индольного гетероцикла, вместо индазольного в структуре MDMB(N)-2201. Структурные формулы каннабимиметиков MDMB-2201 и MDMB(N)-2201 представлены на рисунке 1. Рис. 1. Структурные формулы каннабимиметиков MDMB-2201 и MDMB(N)-2201  Учитывая высокую вероятность географического распространения MDMB-2201 и необходимость его идентификации в биологических объектах с целью установления фактов употребления, изучение метаболического профиля мочи нового каннабимиметика MDMB-2201 является важным для работы экспертных лабораторий. Целью работы является изучение метаболического профиля каннабимиметика MDMB-2201 в моче для целей скрининга с использованием твердофазной экстракции и газовой хроматографии с масс-спектрометрическим детектированием (ГХ/МС). Используемое оборудование, объекты и методы исследования ● Газовый хроматограф с масс-спектрометром Agilent 7820/5975 с колонкой НР-5MS (Agilent, США); ● вакуумный манифолд на 12 образцов (Supelco); ● вакуумный насос KNF lab LABOPORT (Франция); ● термоблок ПЭ-4030 (Россия); ● испаритель одноканальный ПЭ-2300 (Россия); ● микровстряхиватель ПЭ-2 (Россия); ● СВЧ печь Supra MWS-1824SW (Россия); ● патроны SampliQ EVIDEX (200 мг,3 мл) (Agilent, США); ● пипетки-дозаторы полуавтоматические для отбора жидкостей (4-40, 40-200 мкл, 0,2-1, 1-5 мл). ● Семь проб мочи, поступивших в химико-токсикологическую лабораторию от пациентов отделения острых отравлений и освидетельствуемых на состояние опьянения. В исследовании применялись растворители и реактивы чистоты "хч". Образцы мочи до исследования хранились в холодильнике при + 4 оС. Пробоподготовка [1]. Пробоподготовка образцов мочи (с ферментативным гидролизом): к 1 мл мочи добавляли по 50 мкл этанольных растворов внутренних стандартов: гидрохлорид этилморфина (0,02 мг/мл), гексенал (0,2 мг/мл), N-этилбензиламин (0,01 мг/мл). Для одной параллели проб мочи (с ферментативным гидролизом): к пробе мочи добавляли 250 мкл 0,067 М буфера фосфатного (pH 6) и 50 мкл β-глюкуронидазы и выдерживали 2 часа при 45о С. В образцы мочи (с гидролизом и без) вносили 2 мл 0,067 М буфера фосфатного (рН 4.8). После центрифугирования при 3000 об / мин (10 минут) супернатант отделяли от осадка. Сорбент патрона для ТФЭ (смешанная фаза) кондиционировали, пропуская по 2 мл 95% этанола и 0,067 М буфера фосфатного (рН 4.8), пропускали образец (скорость – 1 мл/мин). Для промывки использовали 1 мл 0,067 М буфера фосфатного с рН 4.8, 1 мл 10% этанола. Сушка патрона – под вакуумом (20 минут). Получали два элюата: дважды по 2 мл пропускали элюент гексан – этилацетат (2:1), при этом получали I элюат. Затем при двукратном пропускании через патрон по 2 мл элюента метиленхлорид – 2-пропанол – 25% раствор аммиака (2:1:0.1) получали II элюат. Оба элюата испаряли при 45о С в токе азота. Дериватизация [1]. Получение метильных производных. К сухому остатку первого элюата вносили 500 мкл ацетона безводного, 40 мкл метилиодида, 20-25 мг карбоната калия безводного, нагревали в термоблоке 60 минут при 60о С после герметичного укупоривания. Жидкую фракцию смеси после охлаждения флакона отбирали в чистую виалу, испаряли при 40о С в токе азота. Сухой остаток реконструировали в 100 мкл этилацетата безводного. Получение ацетильных производных. К сухому остатку II элюата или I элюата (последний после процедуры метилирования) добавляли 40 мкл пиридина безводного, 60 мкл ангидрида уксусного, замывая стенки виалы; укупоренную виалу на 5 минут помещали в СВЧ-печь с мощностью 560 Вт. После охлаждения флакона избыток реагентов удаляли не выше 40о С в токе азота. Сухой остаток реконструировали в 100 мкл этилацетата безводного. Триметилсилилирование. К сухому остатку I или II элюатов вносили 100 мкл BSTFA (с 1% триметилхлорсиланом), перемешивали на микровстряхивателе после герметичной укупорки, выдерживали в термоблоке в течение часа при 80о С. После охлаждения виалы 2 мкл вводили в испаритель газового хроматографа. Режим работы ГХ/МС. Поток гелия (газ-носитель) через колонку со скоростью 1,5 мл/мин, испаритель хроматографа работал в режиме split/splitless (при делении потока – 15:1, задержка включения после ввода пробы – 1 мин). Температуры интерфейса детектора и испарителя хроматографа устанавливалась 280 и 250о С, соответственно. Температура колонки: начальная 70о С (2 мин), прогрев до 280о С (скорость программирования – 20 град/мин, 8 мин. – выдержка при конечной температуре). Напряжение на умножителе детектора соответствует показателю автоматической настройки детектора. Масс-спектры ацетильных и метильных дериватов (при полном сканировании ионов) регистрировали в интервале масс 42-450 Да. Масс-спектры триметилсилильных дериватов (при полном сканировании ионов) регистрировали в интервале масс 43-650 Да. Идентификация компонентов проб была проведена с применением программ MSD ChemStation E.02.01.1177 (Agilent) и AMDIS. Долю конъюгирования метаболитов MDMB-2201 для их метиловых эфиров определяли по величине отношения площади пиков иона с величиной m/z: для М 1 и артефакта М8 – 232, M2 и артефакта М9– 230, М3 – 158, М4 – 262, М6 и артефакта М5 – 258, М7.1, М7.2 и М10 – М12 – 188, М13.1 и М13.2 – m/z 248 к площади пика иона m/z 235 для внутреннего стандарта N-метилгексенала в I элюате мочи (с гидролизом и без). Содержание М1 было принято за 100%, расчет значения прочих метаболитов проведен по соотношению площади пиков характеристических ионов со 100% интенсивностью в масс-спектре метаболитов. Расчет констант (LogP, KOC) проведен с применением пакета программ ACD/Labs v6.0. Результаты и обсуждение Химическое название каннабимиметика MDMB-2201 – 2-[1-(5-фторпентил)-1H-индол-3-карбоксамид]-3,3-диметилбутановой кислоты метиловый эфир; брутто формула: C21H29FN2O3; молекулярная масса = 376 г/моль. CAS № 1971007-88-1 Синонимы: 5-fluoro-MDMB-2201, 5-fluoro MDMB-PICA. Структурные формулы предполагаемых метаболитов MDMB-2201, выявленных в реальных пробах мочи, представлены на рисунке 2. Структуры метаболитов определяли на основании данных масс-фрагментации пиков на хроматограммах при анализе мочи потребителей наркотических средств с учетом характерных закономерностей. Для установления типа функциональных групп, имеющихся в структуре метаболитов, получали различные производные метаболитов. На рисунках 3-15 приведены структурные формулы, масс-спектры и аналитические характеристики ряда полученных производных метаболитов MDMB-2201. Рис. 2. Структурные формулы метаболитов MDMB-2201  Рис. 3. Структура, масс-спектр и аналитические характеристики метилового эфира метаболита М1  Рис. 4. Структура, масс-спектр и аналитические характеристики диметилового эфира метаболита М2  Рис. 5. Структура, масс-спектр и аналитические характеристики диметильного производного М3  Рис. 6. Структура, масс-спектр и аналитические характеристики диметилового эфира метаболита М4  Рис. 7. Структура, масс-спектр и аналитические характеристики артефакта метилового эфира метаболита М5  Рис. 8. Структура, масс-спектр и аналитические характеристики диметилового эфира метаболита М6  Рис. 9. Структура, масс-спектр и аналитические характеристики триметильных производных метаболитов М7.1 и М7.2  Рис. 10. Структура, масс-спектр и аналитические характеристики артефакта метаболита М8  Рис. 11. Структура, масс-спектр и аналитические характеристики артефакта метилового эфира метаболита М9 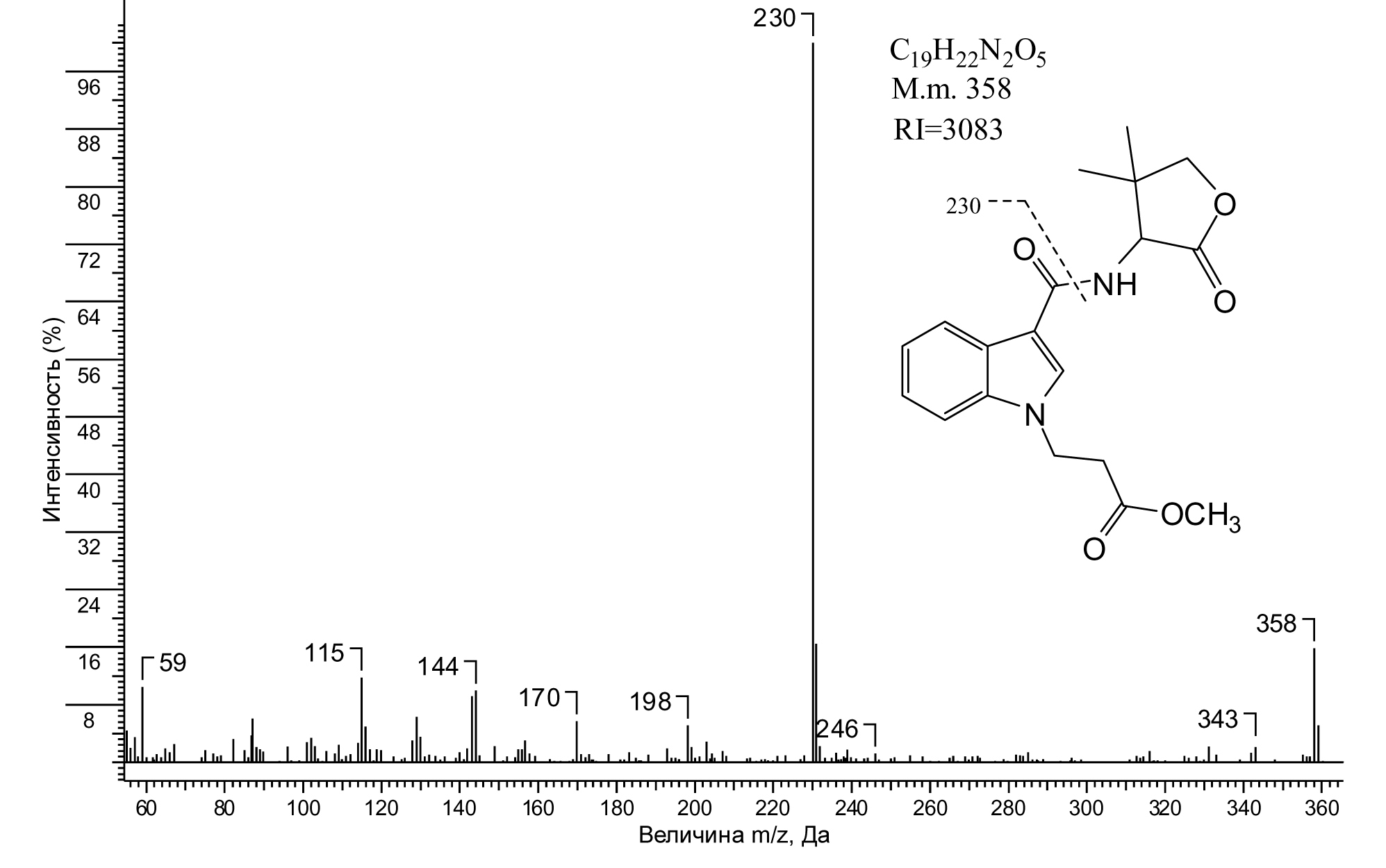 Рис. 12. Структура, масс-спектр и аналитические характеристики метильного эфира метаболитов М13.1 и М13.2  Рис. 13. Структура, масс-спектр и аналитические характеристики метилового эфира метаболитов М13.1 и М13.2 после ацетилирования  Рис. 14. Структура, масс-спектр и аналитические характеристики триметилсильного эфира метаболита М1  Рис. 15. Структура, масс-спектр и аналитические характеристики бис-триметилсилильного производного М3  При исследовании проб с применением различных видов дериватизации метилированием и последующим ацетилированием в двух образцах мочи были идентифицированы метаболиты М13.1 и М13.2, имеющие в структуре соединений спиртовую гидроксильную группу в N-алкильном заместителе. В масс-спектрах метильных производных и артефактов метаболитов MDMB-2201 присутствует молекулярный ион-радикал и ион со 100% интенсивностью, образованный разрывом сигма-связи функциональной группы (амидной или сложноэфирной для М10 – М12) в положении 3. Общим направлением фрагментации, характерным для метиловых эфиров, за исключением метаболитов М10 – М12, является отщепление 2-метилпроп-1-ена, образующегося из трет-бутильного фрагмента с получением ион-радикала [М-56]+. Необходимость проведения гидролиза (ферментативного или щелочного) на предварительной стадии анализа определяется высокой долей конъюгирования маркеров каннабимиметиков; в силу липофильности маркеров их можно выделять, применяя различные гидрофобные сорбенты, либо сорбенты смешанного типа. Последние дают возможность проводить определение маркеров каннабимиметиков в скрининге мочи при поиске наркотических и лекарственных веществ [7]. При использовании на стадии пробоподготовки ТФЭ проведено фракционирование аналитов на фракции кислотного/основного характера. Все выявленные метаболиты MDMB-2201 обнаружены в первом элюате. При исследовании семи проб мочи потребителей MDMB-2201 исходное соединение обнаружено не было. В анализируемых образцах выявлено 15 метаболитов фазы I биотрансформации MDMB-2201, что свидетельствует об интенсивном метаболизме данного каннабимиметика в организме человека. В таблице 1 приведены результаты расчета Log P, Koc (pH=4.8) и оценки относительного содержания, а также степени конъюгации метаболитов MDMB-2201. Из представленных данных видно, что основная доля метаболитов фазы I биотрансформации каннабимиметика элиминируется с мочой в виде конъюгатов, что обусловлено их значительной липофильностью. Таблица 1. Характеристика каннабимиметика MDMB-2201 и его основных метаболитов (n-количество образцов, где было обнаружено соединение)  Основным направлением метаболизма MDMB-2201 является гидролиз сложноэфирной группы с образованием метаболита М1. Последний может быть использован в качестве маркера употребления MDMB-2201 при скрининговом анализе мочи с применением метода ГХ/МС. Значительное содержание наблюдается так же для N-дезалкильного метаболита М3. Прочие метаболиты определяются в моче в незначительных количествах. Метаболиты MDMB-2201 с сохранением сложноэфирной связи в исследованных образцах мочи не выявлены. Метаболиты М10 – М12, образующиеся в результате гидролиза амидной группы в положении 3 индольного гетероцикла, идентичны мочевым метаболитам потребителей PB-22F [8]. Метиловые эфиры метаболитов М5, М8, М9, будучи термолабильными, при ГХ/МС исследовании образуют лактоны (артефакты) вследствие процесса внутримолекулярной циклизации. Заключение В процессе изучения метаболического профиля с использованием ТФЭ и метода ГХ/МС идентифицированы 15 основных метаболитов и маркеров синтетического каннабимиметика MDMB-2201 в моче его потребителей. Основные направления биотрансформации связаны с гидролизом сложноэфирной группы, реакцией N-дезалкилирования и образованием моногидроксилированных производных, которые выводятся с мочой, преимущественно, в конъюгированном виде. Приведены масс-спектры электронной ионизации идентифицированных метаболитов MDMB-2201, результаты расчетов некоторых физико-химические характеристик и степени конъюгации метаболитов. Полученные данные позволяют использовать их при скрининге биологических объектов на наличие синтетических каннабимиметиков. Список литературы 1. Дворская О.Н., Катаев С.С., Мелентьев А.Б. Идентификация маркеров некоторых синтетических каннабиноидов в биологических объектах: Информационное письмо рекомендовано к изданию Ученым советом ФГБУ РЦСМЭ Минздрава России (протокол № 1 от 17 марта 2017 г.). Ижевск. 34 с. 2. Катаев, С.С., Дворская О.Н. Идентификация метаболитов каннабимиметика PB-22F в моче. Бутлеровские сообщения 2014; 37 (2): 114-121. 3. О внесении изменений в некоторые акты Правительства Российской Федерации в связи с совершенствованием контроля за оборотом наркотических средств. Постановление Правительства Российской Федерации от 23.06.2014 г. N 578. URL: http://www.consultant.ru/document/cons_doc_LAW_164873/ 4. Banister S.D., Longworth M., Kevin R., Sachdev S., Santiago M., Stuart J., Mack J.B., Glass M., McGregor I.S., Connor M., Kassiou M. Pharmacology of Valinate and tert-Leucinate synthetic cannabinoids 5F-AMBICA, 5F-AMB, 5F-ADB, AMB-FUBINACA, MDMB-FUBINACA, MDMB-CHMICA, and their analogues. ACS Chem. Neurosci. 2016; 7 (9): 1241-54. doi: 10.1021/acschemneuro.6b00137 5. Hasegawa K., Wurita A., Minakata K., Gonmori K., Yamagishi I., Nozawa H., Watanabe K., Suzuki O. Identification and quantification of 5-fluoro-ADB, one of the most dangerous synthetic cannabinoids, in the stomach contents and solid tissues of a human cadaver and in some herbal products. Forensic Toxicol. 2015; 33 (1): 112-21. 6. Kaneko S. Motor vehicle collisions caused by the 'super-strength' synthetic cannabinoids, MAM-2201, 5F-PB-22, 5F-AB-PINACA, 5F-AMB and 5F-ADB in Japan experienced from 2012 to 2014. Forensic Toxicol. 2017; 35 (2): 244-51. 7. Mogler L., Franz F., Rentsch D., Angerer V., Weinfurtner G., Longworth M., Banister S.D, Kassiou M., Moosmann B., Auwärter V. Detection of the recently emerged synthetic cannabinoid 5F-MDMB-PICA in 'legal high' products and human urine samples. Drug Test Anal. 2018; 10 (1): 196-205. doi: 10.1002/dta.2201 8. Risseeuw M.D.P., Blanckaert P., Coopman V., Van Quekelberghe S., Van Calenbergh S., Cordonnier J. Identification of a new tert-leucinate class synthetic cannabinoid in powder and "spice-like" herbal incenses: Methyl 2-[[1-(5-fluoropentyl)indole-3-carbonyl]amino]-3,3-dimethyl-butanoate (5F-MDMB-PICA). Forensic Sci Int. 2017; 273: 45-52. doi: 10.1016/j.forsciint.2017.01.023
Corresponding Author: Dvorskaya Oksana, e-mail: dvoksnik@gmail.com. Funding. The study had no sponsorship. Conflict of interest: The authors declare no conflict of interest. Abstract The first cases of identifying consumers of cannabimimetics MDMB-2201 during urine testing for narcotic substances in the Russian Federation were registered in March-April 2019 in the cities of Tyumen, Yekaterinburg, and Kurgan., 15 main metabolites and markers of the cannabimimetic MDMB-2201 were identified in the urine of consumers of smoking mixtures using solid-phase extraction and gas chromatography with mass spectrometric detection. Mass spectra of electronic ionization of the identified metabolites of MDMB-2201 were obtained, the results of calculations of several physicochemical characteristics and the degree of conjugation of metabolites to establish the facts of taking the cannabimimetic MDMB-2201 in the analysis of obtained biologic objects are presented. Key words MDMB-2201, cannabimimetics, metabolites, urine, solid-phase extraction (SPE), gas chromatography - mass spectrometry (GC-MS) References 1. Kataev S.S., Dvorskaya O.N., Melent’ev A.B. Identifikatsiya markerov nekotorykh sinteticheskikh kannabinoidov v biologicheskikh ob’yektakh: informatsionnoye pis'mo. [Identification of markers of some synthetic cannabinoids in biological objects: Information letter]. Izhevsk. 2017: 34 p. (In Russ.) 2. Kataev S.S., Dvorskaya O.N. Identifikaciya metabolitov kannabimimetika PB-22F v moche [Identification of PB-22F cannabimimetics’ metabolites in urine]. Butlerovskie soobshcheniya [Butlerov Communications] 2014; 37 (2): 114-21. (In Russ.) 3. O vnesenii izmeneniy v nekotoryye akty Pravitel'stva Rossiyskoy Federatsii v svyazi s sovershenstvovaniyem kontrolya za oborotom narkoticheskikh sredstv: postanovleniye Pravitel'stva Ros. Federatsii ot 23.03.2015 № 578 [On introducing changes to certain cuts of the Government of the Russian Federation due to the improvement of control over the circulation of narcotic drugs: Decree of the Government of Russian Federation from 23 Mar 2015 No 1097]. Available from: http:// www.consultant.ru/document/cons_doc_LAW_164873/ (In Russ.) 4. Banister S.D., Longworth M., Kevin R., Sachdev S., Santiago M., Stuart J., Mack J.B., Glass M., McGregor I.S., Connor M., Kassiou M. Pharmacology of valinate and tert-leucinate synthetic cannabinoids 5F-AMBICA, 5F-AMB, 5F-ADB, AMB-FUBINACA, MDMB-FUBINACA, MDMB-CHMICA, and their analogues. ACS Chem. Neurosci. 2016;7(9):1241-54. doi: 10.1021/acschemneuro.6b00137 5. Hasegawa K., Wurita A., Minakata K., Gonmori K., Yamagishi I., Nozawa H., Watanabe K., Suzuki O. Identification and quantification of 5-fluoro-ADB, one of the most dangerous synthetic cannabinoids, in the stomach contents and solid tissues of a human cadaver and in some herbal products. Forensic Toxicol. 2015; 33 (1): 112-21. 6. Kaneko S. Motor vehicle collisions caused by the 'super-strength' synthetic cannabinoids, MAM-2201, 5F-PB-22, 5F-AB-PINACA, 5F-AMB and 5F-ADB in Japan experienced from 2012 to 2014. Forensic Toxicol. 2017; 35 (2): 244-51. 7. Mogler L., Franz F., Rentsch D., Angerer V., Weinfurtner G., Longworth M., Banister S.D, Kassiou M., Moosmann B., Auwärter V. Detection of the recently emerged synthetic cannabinoid 5F-MDMB-PICA in 'legal high' products and human urine samples. Drug Test Anal. 2018; 10 (1): 196-205. doi: 10.1002/dta.2201. 8. Risseeuw M.D.P, Blanckaert P., Coopman V., Van Quekelberghe S., Van Calenbergh S., Cordonnier J. Identification of a new tert-leucinate class synthetic cannabinoid in powder and "spice-like" herbal incenses: Methyl 2-[[1-(5-fluoropentyl)indole-3-carbonyl]amino]-3,3-dimethyl-butanoate (5F-MDMB-PICA). Forensic Sci Int. 2017; 273: 45-52. doi: 10.1016/j.forsciint.2017.01.023. |
[ См. также ] Рубрики |
||||
|
|
|
Журнал «Медицина» © ООО "Инновационные социальные проекты"
|